|
|
Az angliai Derby katedrálisának délkeleti sarkában
áll a családalapító Elisabeth Hardwick (†1608), Shrewsbury grófnőjéek
(Sir William Cavendish harmadik feleségének) csodaszép síremléke.
Jonathan Powers, a helyi egyetem emeritus filozófiaprofesszora 2010.
február 24-én, pontosan Henry Cavendish halálának 200. évfordulóján
itt tartott másfél órás megemlékezést 187 vetített képpel. A mintegy
száznyolcvan hallgató közt ott voltak a főúri utódok, városi, megyei
előkelőségek. A síremlék melletti falon a leszármazottak nevét
megörökítő 18. és 19. századi bronz feliratok láthatók. Köztük
szerényen húzódik meg a síremlék mögötti Devonshire-i kripta 28.
koporsójáról az 1970-es években kihozott tábla: „HENRY CAVENDISH, Lord
Charles Cavendish (harmadik fia Devonshire második hercegének) idősebb
fia. A Royal Society, a Londoni Történeti Társaság tagja. A British
Museum gondnoka, az Institut de Paris első osztályának kültagja.
Született 1731. október 10-én. Meghalt 1810. február 24-én.”
Henry Cavendish édesanyja, Anne Grey, Henrik kenti
herceg negyedik leánya beteges volt. Házasságkötésük után férjével
Nizzába utazott, hogy ott születhessen meg gyermekük. A neves nizzaiak
közt számon tartják Cavendisht, azonban semmi közelebbit nem sikerült
a születés helyéről és az erre utaló bárminemű emlékállításról
találnunk.
Nizzából hamarosan visszaköltöztek angliai
birtokukra, a hertfordshire-i Putteridge-be, amely félúton volt London
és Cambridge között. Az édesapa felismerte Henry pszichiátriai
problémáit, beteges félénkségét és szégyenlősségét, ezért – egészséges
öccsével együtt − magántanárokkal otthon taníttatta. Henry tizenegy
éves korában kezdte meg tanulmányait a felső osztályok gyermekeinek
kedvelt magániskolájában, a Dr. Newcome Akadémián, Hackney-ben, két
mérföldnyire Londontól északra. Tizennyolc éves korában, 1749.
december 18-án a Cambridge-i Egyetem legrégebbi és legkisebb
kollégiuma, a Peterhouse College felvételi anyakönyvébe nemes
emberként írták be: „Honorabilis Henricus Cavendish, viri Honorissimi
Domini Caroli Cavendish Filius natu maximus…” Cavendish egész életében
nem szerzett rangokat. Az Angol Tudományos Akadémia, a Royal Society
folyóiratában, a Philosophical Transactions-ben (a továbbiakban Phil.
Trans.) tiszteletből eleinte a neve elé tették a Hon. szócskát, később
a neve után az Esq. rövidítést, az ’Úr’ elegáns angol elnevezését. A
Peterhouse-t a Senatus előtti záróvizsga letétele nélkül hagyta el
1753. február 23-án. Ez akkoriban általános volt a második legmagasabb
kollégiumi díjat fizetők, a Fellow Commoner diákok közt. A College
egykori eminens hallgatóinak felsorolásánál szerepel Cavendish, ám –
egy olajfestménytől eltekintve (Schaffer, 2004) − az emlékállításnak
semmilyen más nyomára nem bukkantunk. Pedig kutatási eredményeinek
széles köre és méréseinek pontossága alapján a 18. század második
felében ő volt a legjelentősebb angol természettudós. Megérdemelne egy
ugyanolyan egészalakos szép márványszobrot, mint amilyet az egykori
diák tiszteletére a cambridge-i Trinity College kápolnájában Isaac
Newton kapott. Mintaként szolgálhatna az egyetlen róla készült
műalkotás, egy vízfestmény, amelyet a British Museum grafikai
osztályán őriznek (1. kép). A finom ceruzarajz a kor
portréstílusának megfelelően tustintás árnyalású, egyedül az arcon van
egy kicsi szín. A képet a test felső részéről titokban készítette
William Alexander festőművész, miközben Cavendish klubjában ebédelt. A
többi emlékezetből készült.

1. kép • Henry Cavendish
Cavendish édesanyjának korai halála után apja,
Charles feladta a vidéki birtokot, és 1738-ban Londonba költözött.
Henry cambridge-i tanulmányai befejeztével édesapja westminsteri házát
foglalta el, és ott élt az ő haláláig, 1783-ig. Egészen pontosan a
Blenheim (ma Ramillies) Street sarkán álló, Great Marlborough 13.
számú ház két különálló ingatlan volt, Henry a Blenhem utcára néző
részben lakott. Ez a ház arról nevezetes, hogy 1766-ban Henry
Cavendish itt fedezte fel a hidrogént, és itt végezte elektromos
kísérleteit. Az eredeti ház már nem áll, azonban a kémiai elemek
felfedezéseinek színhelyeit és a felfedezők életét nagy
körültekintéssel és alapossággal kutató két texasi
egyetemi tanár, James és Virginia Marshall a British Museumban talált
régi térképet és egy rajzot is az épületegyüttes hátsó részéről (2.
kép). Rendkívül hálás vagyok nekik, amiért megküldtek minden
Cavendishre vonatkozó anyagot készülő CD-jükről.1 Minden,
Cavendish későbbi lakhelyeire vonatkozó információ tőlük származik.

2. kép • A ház, amelyben Cavendish
felfedezte
a hidrogént és végezte elektromos kísérleteit.
Blaise Pascalhoz, a kimagasló francia kísérleti
fizikushoz hasonlóan Cavendishnek sem volt soha életében kenyérkereső
foglalkozása. Úri kedvtelésből a természetet vizsgálta. Először
édesapjával közösen, majd önállóan. Henry sokoldalú érdeklődését és
szakmai tudásának nagy részét édesapjának köszönheti. Sir Charles
Cavendish tehetséges kísérleti fizikus volt; a hőjelenségekkel, az
elektromossággal és a földmágnességgel foglalkozott. Kísérletező
ügyességét Benjamin Franklin is elismerte egy 1762-ben írt levelében.
A Royal Society már Newton halálának évében, 1727-ben tagjává
választotta az akkor huszonhárom éves Charlest. Tagsága harmincadik
évében saját tervezésű, önregisztráló hőmérőjéért megkapta a Királyi
Társaság legmagasabb kitüntetését, a Copley-érmet. Tudjuk, hogy a
hőmérőt Henry újrakalibrálta 1779-ben; jelenleg Londonban a Royal
Institution tulajdonában van. Charles Cavendish néhány évvel halála
előtt hatalmas vagyont örökölt Elizabeth Cavendishtől (1701− 1779).
Charles halálával ez is Henryre szállt, őt azonban a pénz nem
érdekelte. Csupán annyit tett, hogy 1782 és 1785 között házat bérelt
Hampsteadben, a Church Road 34-ben, ez a ház ma is áll. 1785-ben pedig
egy kastélyba költözött Londontól délre, a Clapham Commonba, s itt élt
haláláig. Ezenkívül fenntartott még egy lakást Londonban, a
Bloomsburyben, a British Museum közelében, a Montague Place és a
Grower Street sarkán, a Bedford Square 11-ben. Itt tartotta hatalmas
könyvtárát és néhány műszerét. Ez a ház is megvan még, rajta díszes
öntöttvas tábla hirdeti: „Itt élt nemes Henry Cavendish
természetfilozófus. Született 1731. Meghalt 1810.” Ezenkívül nem
találtunk Londonban Cavendishhez kapcsolódó, a nevezetes helyeket
manapság jelölő „kék táblát” vagy valamilyen más emlékhelyet, szobrot.
Örömünkre szolgál viszont, hogy Than Károly
(1834−1908), jeles kémikusunk, az MTA rendes tagja, a fiatal Eötvös
Loránd támogatója a Trefort-kerti Vegytani Intézet tervezésekor már
gondolt az emlékállításra, és az épület csodaszép előcsarnokának
falára világhírű kémikusokról kerek terrakotta reliefeket rendelt E.
March-tól 1870-ben. Ott látható ma is a Cavendisht ábrázoló domborműve
többek közt John Dalton, Joseph Priestley, Jöns Jacob Berzelius, Carl
Wilhelm Scheele, Antoine Laurent Lavoisier, Robert Wilhelm Bunsen,
Humphry Davy és Justus von Liebig társaságában.
A különc tudós
Cavendishnek nem voltak társadalmi kapcsolatai. Rendszeresen eljárt a
Royal Society klub heti ebédjeire a Crown and Anchor tavernába,
illetve az akadémiai ülésekre, de csak szakmai kérdésekről
beszélgetett. Vállalt funkciókat, részt vett bizottságok munkájában,
de ezek mindig tudományos érdeklődéséhez kapcsolódtak. Kirándulásai
nem pihenést, hanem kutatási célokat szolgáltak. Két tudóstársával
került szorosabb kapcsolatba. Az egyik Sir Charles Blagden (1748−1820)
a Royal Society titkára, aki évi 500 fontért az asszisztense volt. A
másik John Michell (1724−1793) tiszteletes, az oldatok fagyására
vonatkozó törvényéről ismert matematikus és geológus professzor, a
Cavendish méréseihez használt torziós inga alkotója. Ő jósolta meg
először a fekete lyukak létét is.
Cavendish igazi érdemeit csak jóval halála után
ismerte fel a világ. Nagyon keveset publikált. Ennek nem az volt az
oka, hogy nagyfokú igényessége miatt még csiszolni akarta kéziratait,
hisz azok értékesek, hibátlanok, nyomdakészek voltak. Előfordult, hogy
vitába keveredett megjelent írása miatt, s ez nagyon bántotta. Kerülte
az összeütközést, a vitát, és különben sem érdekelte a hírnév.
Nem érdekelték a nők, nem érdekelte a pénz, sem a
hírnév, a politika, a szépirodalom, a képzőművészet vagy a zene. Ez
nem egy normális állapot. Életrajzírója, George Wilson, a tehetséges
fiziológus és kémikus 1851-ben a Cavendish Társaság kiadásában
megjelent könyvében így jellemezte őt: „…nem szeretett, nem gyűlölt,
nem reménykedett, nem félt, nem járt templomba, mint mások.
Elhatárolta magát a többi embertől és magától az Istentől is.
Természetében nem volt semmi lelkes vagy hősi.” Ez az érzelemmentesség
hasznos is lehet a tudományos kutatásban, hisz így az érzelmek nem
befolyásolják negatív irányban az ítélőképességet. Valóban ekképp
folytatta a jellemzést Wilson: „intellektuális fej a gondolkodáshoz,
két csodálatos éles szem a megfigyeléshez és két nagyon ügyes kéz a
kísérletezéshez vagy a feljegyzéshez.” Ezen jellemzés alapján Oliver
Sachs New York-i neurológus többek közt azt állapította meg, hogy
Cavendish agya számológép, kezei manipulátorok, melyek sosem
reszketnek az érzelemtől, és szíve csupán anatómiai szerv, amely arra
jó, hogy fenntartsa a vérkeringést. Ugyanakkor rendkívüli intuitív
erő, nagy leleményesség és komoly matematikai képesség jellemezte.
Ezek alapján feltételezi, hogy Cavendish esetében az
Asperger-szindróma egy korai esetével állunk szemben, annyira jól
illenek a „tünetek” ebbe a kórképbe.
Cavendish kémiai felfedezései
A reneszánsz majd a barokk kor tudósai rendkívül sokoldalúak voltak,
de kémiával nem foglalkoztak. Nem voltak meg az analizáláshoz
szükségeses mérőeszközök. Maga Newton is, bár szégyellte, csupán az
alkímiát űzte. Az alkimisták elemeket akartak átalakítani anélkül,
hogy tudták volna, hogy mik is az elemek.
A görögök úgy gondolták, hogy a világot alkotó négy
őselem a víz, a tűz, a levegő és a föld. Cavendish ezek közül
kettőről, a vízről és a levegőről bebizonyította, hogy azok összetett
képződmények, sőt kis túlzással azt mondhatjuk, hogy még a tűz
lényegéről is fontos megállapítást tett. Georg Stahl (1660−1734) német
kémikus vezette be a flogiszton misztikus fogalmát. Ő maga azt a tűz
lángjával azonosította, mások a kémiai reakcióban keletkezett hőre
gondoltak. Cavendish is a flogiszton híve volt. Ő azonban azt
állította, hogy ha a flogiszton egyáltalán létezik, akkor az maga a
gyúlékony levegő, azaz a hidrogén. Jóllehet már 1760. május 1-jén
akadémiai tag lett, a gázok vizsgálatáról szóló első nagy művét csak
1766-ban olvasta fel, május 29-én, majd november 6-án és 13-án (Three
Papers Containing Experiments on Factitious Air, Phil. Trans. 1766.
56, 141–184,) Az első rész a gyúlékony levegővel végzett kísérletekről
szólt. Cinket, vasat és ónt oldott hígított kénsavban, sósavban és
salétromsavban. Úgy gondolta, hogy a hidrogén az oldott fémekből válik
ki. Gondos mérésekkel meghatározta, hogy a hidrogén 8760-szor könnyebb
a víznél és tizenegyszer könnyebb, mint a közönséges levegő. A mai
pontos érték 14,4. Nem elmarasztalni kell Cavendisht a mérési hibáért,
hanem dicsérni azért, hogy egyáltalán közölt mérési eredményt.
Módszere nem is tett lehetővé pontosabb mérést. Tanulmányának második
és harmadik része a szén-dioxid vizsgálatával foglalkozik. A
„megkötött” levegőnek nevezett szén-dioxidot alkáli anyagok oldásával,
illetve erjedő, rothadó anyagokból nyerte. A negyedik, publikálatlan
rész fák és állatok desztillálásakor keletkező gyúlékony levegőről
szól. Feltehetően hidrogén, metán és szén-monoxid keverékét kapta.
Megállapította, hogy a desztillálással nyert gyúlékony levegő
különbözik a fémek savakban történő oldásakor kapott gáztól.
Sok mindennel foglalkozott még, mi most csak néhány
jelentős eredményéről szólunk. Nagyon pontosan meghatározta a levegő
összetételét, nemcsak a föld felszínén, hanem légballonosokkal
hozatott mintákat különböző magasságokból. Meghatározta a salétromsav
kémiai összetételét. Kísérletei közben megállapította, hogy a
levegőben a nitrogénen és az oxigénen kívül olyan gáznak is kell
lennie igen kis mennyiségben, amely nem lép kémiai reakcióba. Kis
túlzással azt szokták mondani, hogy Lord Rayleigh (John William
Strutt) és William Ramsay előtt száz évvel felfedezte az argont,
illetve a nemesgázokat.
Hőtani kérdésekkel is foglalkozott: a kémiai
reakcióhő, a fajhő, a latens hő mind-mind érdeklődési körébe
tartozott. Angliában ő fagyasztott meg először
higanyt, hó és hígított salétromsav segítségével. A hőátadás
folyamatát atomi szinten értelmezte.
Joseph Priestleyvel ellentétben Cavendish nem
törődött eszközeinek külalakjával, s minden kísérletéhez új
összeállítást használt (3. kép). Nem az
eredeti, 1766-os, Copley-éremmel jutalmazott írásból, hanem az arra
való hivatkozásból (Greenberg, 2007) vettük a kísérleti
összeállításait bemutató képet.
Két kortárs kémikus, Joseph Black (1728− 1799) és
Joseph Priestley (1733−1804) munkáinak hatására Cavendish 1778-ban
tért vissza a gázok kémiájához, és 1786-ig ezzel foglalkozott. A
korabeli kísérleti eredmények azt mutatták, hogy hidrogénnek levegőben
történő „elégetésekor” a végtermékek össztömege kevesebb, mint a
kiindulási anyagoké. 1871-ben Cavendish üveghengerben „égette el” a
hidrogént, s az edény falán keletkező vékony, folyékony lecsapódási
réteg tömegét is pontosan megmérte, ezzel helyreállt az egyensúly.
Kimérte, hogy az elektromos szikrával történő robbantáskor (így
történt az „elégetés”) az összes gyúlékony levegő és a közönséges
levegő egyötöde alakul nedvességgé. Gondos vizsgálatokkal kimutatta,
hogy az üveghenger falán keletkezett folyadék tiszta víz! (4. kép)
Az oxigén az ő fogalomrendszerében a flogisztonjától megfosztott víz,
tehát a víz oxigénből és hidrogénből összetett anyag. Cavendish
eredményeit szóban közölte kollégáival, ám az Experiments on Air című
munkáját csak 1784. január 15-én olvasta fel akadémiai ülésen (Phil.
Trans. 1784, 74, 119–169.), ezért sok kutató, köztük Lavoisier is azt
állította, hogy ő állapította meg a víz összetételét. A víz
elektrolízissel történő felbontása csak a Volta-oszlop, az elektromos
telep 1800-as felfedezése után vált lehetővé.
|
|
|

4. kép • Üveg és fém eudiométer, amelyekkel
Cavendish felfedezte a víz összetételét
A hidrogén felrobbantására szolgáló, ún. eudiométer
bronz változatát Sir Humphry Davy ajándékozta a Royal Institute-nak,
feltehetően először ezzel kísérletezett Cavendish. Ami csaknem
bizonyosan az ő készüléke volt, és a tanulmányában leír, az üvegből
készült, és jelenleg a Manchesteri Egyetem Kémiai Tanszékén található.
Frederick Seitz (2004) így fogalmaz: „Cavendish
nyitotta ki azt a kaput, amelyen át Lavoisier ellovagolhatott »a
modern kémia atyja« címhez.” Justus von Liebig (1803−1873) szerint
„Lavoisier a tudomány testébe új lelket öntött, azonban ez a test
(elsősorban Cavendish munkássága alapján) már létezett.”
Cavendish fizikai eredményei
Cavendish két kémiai kutatási periódusa közt elektromossággal
foglalkozott. Ha minden elért eredményét publikálta volna, akkor a
diákok ma nem Ohm-törvényről, Coulomb törvényéről tanulnának, nem
Faraday nevéhez kötnék a fajlagos dielektromos állandó fogalmát, sőt,
még tovább menve nem Hermann Ludwig von Helmholtz, James Prescott
Joule és Robert Mayer lennének az energiamegmaradás törvényének
felfedezői. Minderről azonban csak 1879-ben szerezhetett tudomást a
világ. A kísérleti fizika első Cavendish-professzora, az 1874-ben
megnyílt cambridge-i Cavendish Laboratórium első igazgatója, James
Clerk Maxwell (1831−1879) kötelességének érezte, hogy feldolgozza nagy
elődjének munkásságát. Kiadta a W. Snow Harris és William Thomson
(Lord Kelvin) közvetítésével hozzá eljutott kéziratokat. Ráadásul
Maxwell modern eszközökkel megismételte Cavendish méréseit. Azt
mondják, nincs arra még egy példa, hogy valaki ilyen alapossággal
foglalkozott volna elődje munkásságával.
Cambridge-ben a Cavendish Laboratóriumot tehát nem
Henry alapította. Ő azt vallotta, hogy vagyonát őseitől kapta, így azt
a rokonaira hagyja. A Cambridge-i Egyetem kancellárja 1861-től
Devonshire hetedik hercege, William Cavendish (1808−1891), Henry
nagyapjának közvetlen leszármazottja volt. Ő úgy érezte, hogy a
hatalmas vagyonból méltó emléket kell állítani a család
legnevezetesebb tudós tagjának. Felajánlott 6300 fontot fizikai
laboratórium létesítésére.
Henry Cavendish húsznál kevesebb publikációja közül
elméleti munka csak egy van: An Attempt to Explain Some of the
Principal Phaenomena of Electricity by Means of an Elastic Fluid
(Phil. Trans. 1771. 61, 584–677.). Ebben, és még inkább azt ezt
megelőző, Thoughts Concerning Electricity című kéziratában kifejti,
hogy az elektromosságot a test részecskéi között rugalmas folyadéknak
kell tekintenünk. Ez, mint atmoszféra, még a testen kívül is
megtalálható, hatása pedig a testektől igen távol is kimutatható.
Világos „potenciál” fogalma volt, bár ő az ekvipotenciális felületeket
azonos „sűrítettségűnek” nevezte.
Kéziratban maradt az a mérési eredménye is, amely
egy gömb és egy vele azonos potenciálra hozott sík körlap töltése,
illetve kapacitása közt fennálló arányra vonatkozik. A mért hányados
1,57, a pontos elméleti érték π/2 = 1,571…
Az elektromos töltések közt fennálló, a távolság
négyzetével fordítottan arányos erőről szóló törvényt, a
Coulomb-törvényként ismert összefüggést Priestley elméleti úton
megkapta 1767-ben. Ő abból a kísérleti tényből indult ki, hogy
egyrészt a töltések a vezető felületén helyezkednek el, másrészt
üreges vezető belsejében nem észlelhető elektromos erőhatás. A
felületen elhelyezkedő töltések csak akkor rontják le egymás hatását a
zárt felület belsejében, ha a köztük levő erőhatás távolságuk
négyzetével fordítva arányos. Cavendish természetesen mért.
Könyvszerűen összehajtható két félgömb-héjat készített kartonpapírból,
s ennek belsejébe viasszal bevont üveggömböt tett (5. kép). Az
egész rendszer elektromos feltöltése, majd a gömbhéjak szétválasztása
után a belső gömb felületén a félgömbökön levő töltés 1/60 részénél
kevesebb töltés maradt. Csodálatra méltó a mérés és a pontos
fogalmazás: nem azt állítja, hogy a szorosan, egy teljes gömbbé
összezárt, külső, töltött gömbhéj belsejében egyáltalán nem marad
töltés. Megmondja, hogy ezt az elméleti tényt ő milyen pontosan tudta
1772 decemberében méréseivel igazolni!
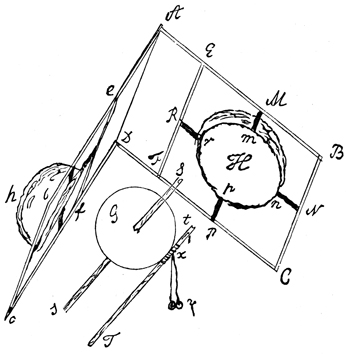
5. kép • Gömbhéj belsejében levő elektromos
töltés vizsgálatára szolgáló eszköz rajza
Az Ohm-törvény megsejtésekor feltöltött leydeni
palackot használt feszültségforrásként, az árammérő pedig a saját
teste volt. (Ne feledjük, hogy ekkor még nem alakult ki az „elektromos
áram” és az „ellenállás” fogalma, s természetesen galvanométer sem
létezett.) A különböző mértékben feltöltött leydeni palackokat a saját
testén keresztül sütötte ki, s megállapította, hogy a feltöltés
mértékével arányos az a hosszúság, ameddig fájdalmat érez karjaiban.
Kontrollmérésként szolgájának, Richardnak az övével
megegyező vélekedése szolgált. Ugyane módszerrel vizsgálta nagy
gondossággal sóoldatok vezetőképességét a koncentráció és a
hőmérséklet függvényében (6. kép). Egy
yardnyi hosszúságú üveg két végébe vezetéket tett, ezek
elhelyezkedésével tudta a vezető oldat hosszát változtatni. Sorba
kötötte az oldatot a testével, és ha azonosan feltöltött leydeni
palackok kisütésekor azonos áramütést érzett, akkor mondta az
ellenállásokat azonosaknak. Fémek ellenállását is mérte.
Megállapította például, hogy „a vashuzal négyszázmilliószor jobban
vezet, mint a desztillált víz”.
Hosszasan foglalkozott az elektromos rája (Raja
torpedo) „működésével”. Anatómiailag John Hunter írta le a torpedót.
Cavendish bőrrel bevont üvegből mesterséges ráját készített.
Feltöltött leydeni palack szolgáltatta a szükséges feszültséget.
Laborjában Hunternek és Priestleynek is megmutatta művét, ők is
„élvezhették” az áramütést. Maxwell megismételte a kísérletet, ő
nedves homokba ágyazta a mesterséges ráját, s arra rálépve a talpon
keresztül lehetett észlelni a hatást.
A Cavendish-kísérlet
Így ismeri a világ, ilyen elnevezéssel. Henry Cavendish volt az első,
aki kézzelfogható földi tárgyak között ki tudta mutatni a
kölcsönhatást, amelyet Newton fogalmazott meg mint az általános
tömegvonzás törvényét. Láttuk, hogy már a Coulomb-törvény kimondásánál
is segített az analógia, a távolság négyzetével fordítottan arányos
erő feltételezése.
Cavendish hatvanhét éves, amikor ezeket a méréseket
végzi. A cél nem a törvény igazolása, nem a tömegvonzás univerzális
állandójának, az f = 6,67·10-11 m3/kg·s2
értéknek a meghatározása volt. „Megmérni a csillagok tömegét!” − ez
lebegett a 18. századi tudósok előtt. Ehhez először a Föld tömegét
kellett meghatározni. Különös módon végső eredményként nem is a tömeg
nagyságát, hanem a Föld átlagos sűrűségét számították ki. A
Philosophical Transactions of the Royal Society London 1798-ban
megjelent 88. kötete 469–526. oldalainak élén ez a cím áll: XXI.
Experiments to determine the Density of the Earth, By Henry Cavendish,
Esq. F. R. S. and A. S., azaz A Föld sűrűségének meghatározására
szolgáló kísérletek.
A Cavendish-kísérlet módszere és az eredeti
mérőeszköz, mint említettük, John Michelltől származik. Michell a
mérés alapötletét − azt, hogy torziós ingát kell használni, és a
torziómoduluszt a lengésidőből kell meghatározni − már Coulomb ilyen
jellegű elektrosztatikus méréseinek publikálása előtt elmondta
Cavendishnek. Mérni azonban nem tudott, mert időközben meghalt. Henry
Cavendish felújította, jelentősen átalakította az eredeti ingát.
Nagy-nagy körültekintéssel végezte a méréseket. Rendkívül gondosan
elemezte a lehetséges hibaforrásokat. Ellenőrző mérésekkel, részletes
számításokkal igazolta, hogy mely hatások hanyagolhatóak el. Becslést
adott a nem mérhető és pontosan ki sem számítható hatásokra. Isobel
Falconer, a cambridge-i Cavendish Laboratórium múzeumának egykori
kurátora Cavendish dolgozatát a hibákról szóló értekezésnek
(„dissertation on errors”) tartja.
Ahogyan Tycho de Brahe csillagászati
megfigyeléseinél, Cavendish méréseinél is döntő szerep jutott a nagy
méreteknek. Az ezüstözött réz torziós szál közel egy méter, az inga
teljes lengő karja 186 cm hosszú, a kar végeiről lelógó fonálra
függesztett ólomgolyók egyenként 0,75 kg tömegűek voltak. A vonzó
ólomgömbök tömege egyenként 168 kg volt. Nem találtuk nyomát annak,
hogy az eredeti mérőberendezést vagy annak részeit valahol őriznék. A
londoni Science Museumnak van egy modellje, amely jelenleg a Kis és
Közepes Eszközök Raktárában, a Blyte House-ban van (7. kép).

7. kép • A Cavendish-féle torziós inga
modellje
a londoni Science Museumban
Cavendish a hosszú lengő kar és a végeiről lelógó
nagy tömegek miatt külön ezüst feszítőhuzalt is alkalmazott. Az egész
ingát mahagóni dobozba zárta be. Charles Coulomb és Eötvös Loránd is a
lengő kar közepére helyezett tükör közvetítésével távcsővel olvasta le
a kar elfordulását. Cavendishnél nem fény, hanem maga a 93 cm hosszú
félkar volt a mutató. A mahagóni doboz minkét végébe nyílást vágott,
ezt üveglemezzel lezárta. A doboz belsejében a karhoz lehető
legközelebbi helyen elefántcsont főskálát helyezett el, egy hüvelyket
(2,54 cm) húsz egyenlő kis részre osztott. A kar végére ugyancsak
elefántcsontból segédskálát tett, amelyen egy kis osztásrészt további
öt egyenlő részre osztott. Így század hüvelyk, azaz 0,25 mm
pontossággal tudta a kar helyzetét meghatározni. Külön szoba közepén
állt Clapham Common-i kastélyában a mahagóni doboz. A falba vágott
résen át, kondenzorlencsén keresztül vetődött fény a skálákra, és
ugyancsak kívülről, távcsővel történt a leolvasás. A vonzó tömegek
lefelé fordított, szögletes U-alakú, felül fával megerősített vasrúdon
lógtak, csiga és fonal segítségével kívülről lehetett azokat
„negatív”, „középső” és „pozitív” helyzetbe állítani. A főskála
beosztása jobbról balra növekedett, ezért a tömegeknek a bal oldali
elhelyezkedését nevezte pozitív helyzetnek. Kívülről lehetett
beállítani az inga szálának s ezzel a rúdnak az alaphelyzetét. Mint
említettem, az inga lengésidejéből számította ki a torziós szál
csavarodási erősségét, a torziómoduluszt. A lengésidő mérését mind a
tizenhét méréssorozatnál újra és újra elvégezte. Azért tette ezt, hogy
az esetlegesen fellépő hibákat ezzel is csökkentse. Példaként említi,
hogy ha a fatok végébe tett üveg elektrosztatikusan feltöltődik, akkor
ez olyan hatású lesz, mintha a torziómodulusz változott volna meg. Ezt
mérésével figyelembe tudja venni. Így már csak az a hiba marad,
amelyet a feltöltött üveglapnak a golyókra gyakorolt hatása okoz. Ezt
nem tudja mérni vagy számolni. A lengésidőt a nyugalmi helyzeteken
történő áthaladások abszolút idejéből határozta meg. A nyugalmi
helyzetek értékeit a szélső helyzetek értékeiből igen gondos
számítással nyerte. Általában öt−tíz lengés együttes idejének átlagát
vette. Három méréssorozatot végzett a kapott, meglevő gyengébb
szállal, és közel 15 perces lengésidőket mért. Ezután erősebb szálra
váltott, közel hétperces lengésidőkkel dolgozott az elkövetkező 14
méréssorozatnál. A tizenhét méréssorozatból összesen 29 sűrűségértéket
számított ki. Az értékek 4,88 és 5,85 g/cm3 közé estek, az átlag 5,48
g/cm3. „A maximálistól való eltérés az utolsó 23
megfigyelésnél 0,38, azaz 1/14.” − írja. Tehát maximális hibája 7%. Az
átlag az eltérések átlagától azonban csak 1%-kal tér el. Sokkal
lényegesebb, hogy Cavendish sűrűségértéke és az abból meghatározható
általános tömegvonzási állandó a mai eszközökkel meghatározott
értéktől is csak 1%-kal tér el!
Cavendish igen jelentős kémiai eredményeket ért el,
de a tömegvonzási erő gondos kimérését s ezzel a Föld sűrűségének
pontos meghatározását tartják a legnagyobb érdemének. Ám ne feledjük,
hogy hihetetlen gondossága kémiai kísérletei közben alakult ki.
Kulcsszavak: fizikatörténet, kémiatörténet, elektromosság, Föld,
hidrogén, víz
IRODALOM
Berry, A[rthur] J[ohn] (1960): Henry
Cavendish, His Life and Scientific Work, Hutchinson, London
Falconer, Isobel (1999): Henry Cavendish:
The Man and the Measurement . Measurement Science and Technology, 10,
470–477.
Greenberg, Arthur (2007): From Alchemy to
Chemistry in Picture and Story, Wiley, Hoboken–New Jersey
Kunfalvi Rezső (1977): Cavendish, Henry.
Tudósok-történetek. Természet Világa. 2, 51.
Maxwell, James Clerk (ed.) (1879): The
Electrical Researches of the Honourable Henry Cavendish, F. R. S.,
Cambridge
McCormmach, Russell (1971): Cavendish,
Henry. In: Dictionary of Scientific Biography. Charles Scribner’s
Sons, New York, 155–159.
Sachs, Oliver (2001): Henry Cavendish: An
Early Case of Asperger’s syndrome? Neurology. 57, 7, 1347.
Simon Schaffer (2004): Cavendish, Henry
(1731–1810). In: Oxford Dictionary of National Biography, Oxford
University Press
WEBCÍM >
Seitz, Frederick (2004): Henry Cavendish:
Catalyst for the Chemical Revolution. Proceedings of the American
Philosphical Society. 148, 151-176. http://www.google.hu/ Books +
Seitz + Cavendish vagy Reprint: Seitz, Frederick (2005): Henry
Cavendish: The Catalyst for the Chemical Revolution. Notes & Records
of The Royal Society. 59, 2, 175–199.
WEBCÍM >
LÁBJEGYZETEK
1 Marshall, James –
Marshall, Virginia: Rediscovery of Elements. <
|
|